Tacrolimus
Le Tacrolimus, aussi connu sous le nom de FK-506 ou de Fujimycine, est un immunosuppresseur utilisé essentiellement en transplantation d'organes pour la prévention du rejet des allogreffes et en dermatologie.
| Tacrolimus | |
|---|---|
  |
|
| Général | |
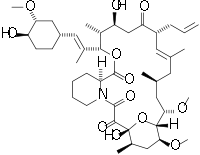
| Nom IUPAC | 3S-[3R*[E (1S*, 3S*, 4S*) ], 4S*, 5R*, 8S*, 9E, 12R*, 14R*, 15S*, 16R*, 18S*, 19S*, 26aR*]] -5, 6, 8, 11, 12, 13, 14, 15, 16, 17, 18, 19, 24, 25, 26, 26 a-hexadecahydro-5, 19-dihydroxy-3-[2- (4-hydroxy-3-methoxycyclohexyl) -1-methylethenyl]-14, 16-dimethoxy-4, 10, 12, 18-tetramethyl-8- (2-propenyl) -15, 19-epoxy-3H-pyrido[2, 1-c] [1, 4] oxaazacyclotricosine-1, 7, 20, 21 (4H, 23H) -tetrone, monohydrate |
| Synonymes | FK-506, Fujimycine |
| No CAS | |
| Code ATC | |
| PubChem | |
| SMILES |
|
| InChI |
|
| Propriétés chimiques | |
| Formule brute | C44H69NO12 [Isomères] |
| Masse molaire | 804, 0182 g∙mol-1 C 65, 73 %, H 8, 65 %, N 1, 74 %, O 23, 88 %, |
| Classe thérapeutique | |
| Immunosuppresseur Inhibiteur de la calcineurine |
|
| Données pharmacocinétiques | |
| Biodisponibilité | 20 % |
| Liaison protéique | 75 - 99 % |
| Métabolisme | Hépatique (CYP3A4) |
| Demi-vie d'élim. | 11, 3 h (3, 5 - 40, 6) |
| Excrétion | Fécale principalement |
| Considérations thérapeutiques | |
| Précautions | Néphrotoxicité |
| Antidote | Orale Intraveineuse Topique |
|
|
|
Le Tacrolimus, aussi connu sous le nom de FK-506 ou de Fujimycine, est un immunosuppresseur utilisé essentiellement en transplantation d'organes pour la prévention du rejet des allogreffes et en dermatologie. Isolé en 1984 dans un échantillon de sol du Japon, le tacrolimus est un macrolide du genre des lactones synthétisé par une bactérie, Streptomyces tsukubænsis. Il appartient comme la ciclosporine à la famille des inhibiteurs de la calcineurine et déprime l'activité des lymphocytes T.
Histoire
Le tacrolimus a été découvert en 1987 par une équipe japonaise dirigée par T. Goto, T. Kino et H. Hatanaka. Il fait partie des premiers macrolides immunosuppresseurs découverts, précédé en 1975 par le sirolimus (ou rapamycine), isolé sur l'île de Pâques. [1] Comme la ciclosporine il a été identifié dans le sol où il est synthétisé par une bactérie, ''Streptomyces tsukubænsis. [2] Le nom tacrolimus est constitué à partir de Tsukuba macrolide immunosuppressant.
La molécule est la propriété de Astellas Pharma et est commercialisée sous les noms de Prograf ®, Advagraf® et Protopic®. Le tacrolimus a été autorisé aux États-Unis par la FDA en 1994, originellement pour la prévention du rejet des allogreffes hépatiques, puis son indication s'est étendue aux allogreffes de rein, de cœur, d'intestin grêle, de pancréas, de poumon, de trachée, de peau, de cornée, de mœlle osseuse et de membre.
Pharmacologie
Pharmacodynamie
Le mode d'action du tacrolimus reste imparfaitement connu. Dans le cytosol des lymphocytes T il se lie à l'immunophiline FKBP-12 (ou FK-506 binding protein) pour former un complexe à 5 sous-unités (une protéine de liaison, le tacrolimus, la calmoduline et les calcineurines A et B) dont le rôle est d'inhiber l'activité phosphatase de la calcineurine. Cette inhibition conduit au blocage de la prolifération des cellules T et de la du gène de l'interleukine 2[3], conduisant à une réduction marquée de l'activité des lymphocytes T effecteurs. Quoique ce mode d'action soit comparable à celui de la ciclosporine A, une étude a prouvé une efficacité supérieure du tacrolimus dans la prévention du rejet aigu. [4]
Pharmacocinétique
Absorption
L'absorption du tacrolimus a lieu à l'ensemble des niveaux du tractus digestif. La résorption est présente de grandes variations inter et intra-individuelles, mais elle est augmentée à jeun. La biodisponibilité de la forme orale fluctue par conséquent de 5% à 67% et est en moyenne de 20 à 25 %.
Distribution
Le volume de distribution du tacrolimus est particulièrement élevé (plus de 1300 litres). À cause de la grande hydrophobie de la molécule, sa distribution se fait en particulier dans les lipides. Les concentrations dans le poumon, la rate, le cœur, le rein et le pancréas après l'équilibre de distribution sont nettement supérieures aux concentrations plasmatiques, indiquant ainsi une grande affinité tissulaire.
Des études ont montré que le sang total est un échantillon meilleur que le plasma pour étudier la pharmacocinétique du tacrolimus. En effet, il se lie aux érythrocytes ainsi qu'aux protéines, en particulier l'albumine et l'α1-glycoprotéine acide. La distribution entre le plasma et les érythrocytes est affectée par plusieurs paramètres : l'hématocrite, la température de séparation du plasma, la concentration du tacrolimus et la concentration des protéines plasmatiques.
Sa grande hydrophobie lui sert à traverser la barrière hémato-encéphalique mais aussi la barrière placentaire. Il est par conséquent excrété dans le lait maternel et est contre-indiqué en cas d'allaitement.
Métabolisme
Il est hépatique à plus de 99 % par la voie du cytochrome P450, isoforme CYP-3A4. Les métabolites du tacrolimus ne sont pas actifs.
Élimination
La demi-vie du tacrolimus est particulièrement variable. Particulièrement élevée chez le sujet sain (pouvant dépasser les 40 heures), elle se situe entre 5, 6 et 16, 6 heures chez le transplanté car la clairance du médicament est augmentée. Le médicament est éliminé presque exclusivement dans les fécès.
Effets indésirables et interactions
Comme la ciclosporine, le tacrolimus est néphrotoxique, hépatotoxique et expose au risque de maladies opportunistes (infections surtout virales et fongiques, et cancers). Les autres effets indésirables sont particulièrement variés et non spécifiques. Le tacrolimus facilite le diabète sucré.
Le tacrolimus interagit avec plusieurs médicaments : les inhibiteurs du cytochrome P450 augmentent sa concentration sérique et son activité : érythromycine et autres antibiotiques macrolides, antifongiques azolés, jus de pamplemousse, etc. ; les activateurs du cytochrome P450 diminuent sa concentration sérique et son activité : rifampicine, millepertuis, phénobarbital, etc.
Indications
Prévention du rejet d'allogreffe
Le tacrolimus a des propriétés immunosuppressives analogues à celles de la ciclosporine, mais il est bien plus puissant à volume égal. Une étude de 2004 a montré sa supériorité sur la ciclosporine dans la prévention du rejet aigu d'allogreffes rénales (30, 7 % contre 46, 4 %). [5] Il possède une indication dans la grande majorité des transplantations.
Dermatologie
En pommade (Protopic ®), le tacrolimus est indiqué dans le traitement de l'eczéma et surtout de la dermatite atopique. Son effet anti-inflammatoire est comparable à celui d'un dermocorticoïde de puissance moyenne à forte. Comparé aux stéroïdes il présente l'avantage d'une meilleure tolérance locale, donnant la possibilité son utilisation sur les surfaces généralement contre-indiquées aux dermocorticoïdes (surtout le visage). Le tacrolimus topique pourrait aussi avoir une efficacité dans le traitement de certaines formes de vitiligo chez les enfants, en particulier sur le visage. [6]
Autres usages
La tacrolimus est à l'étude pour le traitement des formes réfractaires de maladie de Crohn et de rectocolite hémorragique. [7]
Méthodes de dosage dans le sang
Les méthodes de dosage du tacrolimus ont été récemment révisées (1997). La mesure plasmatique ou sanguine est compliquée par les propriétés physico-chimiques spécifiques de la molécule. Ainsi, elle est insoluble dans l'eau, soluble dans les lipides, le méthanol, le chloroforme, l'acétate d'éthyle, l'éther et l'acétone. La molécule ne possède pas de noyau chromophore et n'est pas fluorescente. Quoique complexe à mesurer, la molécule de tacrolimus présente une stabilité intéressante : 1 semaine dans le sang à 25 °C et plus de 6 mois au congélateur.
Les premières méthodes de mesure se basaient sur la réaction lymphocytaire (MLR), peu sensible. Particulièrement vite, une méthode ELISA fut développée pour l'évaluation clinique du médicament. Pour les études pharmacocinétiques, à cause du manque de sensibilité de l'ELISA, on a dû s'en remettre à la technique de HPLC-MS. Puis, en 1991, la compagnie Abbott a introduit une technique fluorescente à microparticules. Cette technique est semi-automatisée avec l'appareil IMx. Ce dernier manquait au début de sensibilité et de précision, et cette faiblesse limitait sérieusement l'application de la technique, puisque les concentrations visées par les cliniciens sont assez basses. Après une actualisation de la technique (Tacrolimus II®), la sensibilité s'est largement perfectionnée (1 à 30 ng/ml) et la précision est acceptable (CV de 8 à 12%). L'avantage majeur de la technique mise au point par Abbott réside dans la rapidité d'exécution et le coût assez faible de l'analyse.
Il faut savoir qu'il existe aussi des techniques HPLC pour la mesure du tacrolimus. Ces mesures doivent être effectuées en tandem avec la spectrographie de masse ou avec une détection par immunœnzymologie. Elles sont longues, laborieuses et par conséquent peu pratiques pour une application de routine avec un volume quotidien élevé de spécimens.
Il forme une alternative à la ciclosporine, dont l'activité in vitro est 100 fois moins puissante ! L'absorption digestive et la pharmacocinétique du tacrolimus présentent une grande variabilité inter- et intra- individuelle, aussi est-il recommandé d'ajuster les posologies par un suivi des concentrations sanguines.
Références
- ↑ (en) Kino T, Hatanaka H, Hashimoto M, Nishiyama M, Goto T, Okuhara M, Kohsaka M, Aoki H, Imanaka H, «FK-506, a novel immunosuppressant isolated from a Streptomyces. I. Fermentation, isolation, and physico-chemical and biological characteristics. », dans J Antibiot (Tokyo) , vol. 40, no 9, 1987, p. 1249-55
- ↑ (en) Pritchard D, «Sourcing a chemical succession for cyclosporin from parasites and human pathogens. », dans Drug Discov Today, vol. 10, no 10, 2005, p. 688-91
- ↑ (en) Liu J, Farmer J, Lane W, Friedman J, Weissman I, Schreiber S, «Calcineurin is a common target of cyclophilin-cyclosporin A and FKBP-FK506 complexes. », dans Cell, vol. 66, no 4, 1991, p. 807-15
- ↑ (en) Long-Term Graft Survival In Kidney Transplant Recipients
- ↑ (en) Long-Term Graft Survival In Kidney Transplant Recipients
- ↑ (en) Nanette B. Silverberg, Peggy Lin, Lisa Travis, Jeanne Farley-Li, Anthony J. Mancini, Annette M. Wagner, Sarah L. Chamlin and Amy S. Paller (Nov. 2004). "Tacrolimus ointment promotes repigmentation of vitiligo in children : A review of 57 cases". Journal of the American Academy of Dermatology, Volume 51, Issue 5, Pages 760-766.
- ↑ (en) Benson A, Barrett T, Sparberg M, Buchman AL, Efficacy and safety of tacrolimus in refractory ulcerative colitis and Crohn's disease : a single-center experience, Inflamm Bowel Dis. 2008 Jan;14 (1) :7-12.
Recherche sur Google Images : |
|
"Tacrolimus has an empirical" L'image ci-contre est extraite du site fujisawa.com Il est possible que cette image soit réduite par rapport à l'originale. Elle est peut-être protégée par des droits d'auteur. Voir l'image en taille réelle (297 x 276 - 7 ko - gif)Refaire la recherche sur Google Images |
Recherche sur Amazone (livres) : |
Voir la liste des contributeurs.
La version présentée ici à été extraite depuis cette source le 10/11/2009.
Ce texte est disponible sous les termes de la licence de documentation libre GNU (GFDL).
La liste des définitions proposées en tête de page est une sélection parmi les résultats obtenus à l'aide de la commande "define:" de Google.
Cette page fait partie du projet Wikibis.


 Accueil
Accueil Recherche
Recherche Début page
Début page Contact
Contact Imprimer
Imprimer Accessibilité
Accessibilité